
Endoprothetik des Hüftgelenkes
Das Deutsche Zentrum für Oberflächenersatz an den DRK Kliniken Berlin bestand von 2003 bis 2012.
Durch die Spezialisierung der Operateure auf den Oberflächenersatz (Birmingham Hip Resurfacing) und den Hüftkopf-Teilersatz (Birmingham Mid Head Resection) verfügte das Zentrum über die Erfahrung von über 2.500 BHR- und über 450 BMHR- Implantationen allein bis 2009.
Auf Grund dieser großen Erfahrung war das Zentrum als Ausbildungsklinik für die Originalverfahren nach McMinn anerkannt und wurde von zahlreichen Ärzten aus dem In- und Ausland besucht.
Die Implantation von Standardprothesen kam zur Anwendung, wenn die beiden knochensparenden Verfahren nicht möglich waren.
Im März 2012 endete mein Vertrag mit den DRK-Kliniken Berlin, seitdem bin ich als Belegarzt tätig. Der BHR – Oberflächenersatz wird aber weiterhin im DRK-Klinikum Westend angewendet.
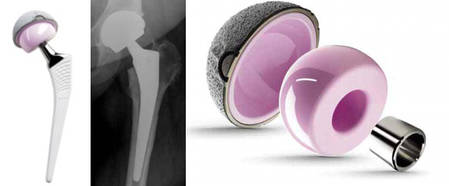
Abbildungen 1a und 1b zeigen im Schema die Versorgungsmöglichkeiten mit knochensparenden Hüftgelenksprothesen.
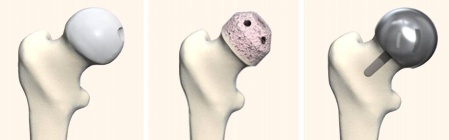
- Abb. 1a
Birmingham Hip Resurfacing (BHR)
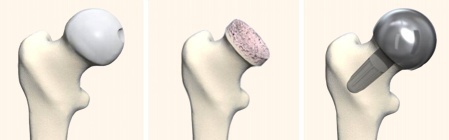
- Abb. 1b
Birmingham Mid Head Resection (BMHR) diese Prothese steht nicht mehr zur Verfügung, weil es zu wenig Anwender gab. Die Ergebnisse damit waren gut.
1. Oberflächenersatz nach McMinn - Birmingham Hip Resurfacing (BHR)

- BHR
Im Gegensatz zu Standardprothesen werden bei diesem Verfahren nur die erkrankten oberflächlichen Anteile des Gelenkes entfernt. Hüftkopf und Schenkelhals bleiben erhalten. Die „Überkronung“ des Hüftkopfes erfolgt mit einer Metallkappe, die - wie auch die dünnwandige Pfanne - aus einer speziellen Kobalt-Chrom-Molybdän-Legierung mit hohem Kohlenstoffgehalt besteht. Die Herstellung und Bearbeitung dieser Gusslegierung entspricht den Metall-Metall Prothesen von Peter Ring (1964) und McKee-Farrar (1966), die in Einzelfällen mehr als 30 Jahre ohne relevanten Abrieb und Zeichen von Lockerung blieben.
Die Primärstabilität wurde mit einer sehr empfindlichen Methode mit Hilfe von Röntgenbildern und Markern über einen Zeitraum von fünf Jahren kontrolliert. Diese Röntgen stereophotogrammetrischen Analysen (RSA) zeigten eine im Vergleich zu Standardschäften deutlich geringere Bewegung. Dieses Ergebnis spricht für eine gute Langzeitstabilität (23,25).
Vorteile gegenüber Standardprothesen:
- Keine wesentliche Änderung der Beinlänge und der Hebelverhältnisse für die Hüftmuskulatur
- Das „Gefühl“ für das Gelenk (Propriozeption) wird kaum beeinflusst.
- Die beinahe natürliche Größe der Implantate erlaubt häufig ein natürliches Bewegungsausmaß und hohe Luxationssicherheit.
- Die natürliche Krafteinleitung vom Becken auf den Hüftkopf und Oberschenkelknochen führt nicht zu Um- und Abbau von Knochen, sondern der durch Schonung verminderte Kalksalzgehalt des Knochens nimmt wieder zu. Der Nachweis erfolgte durch vergleichende Knochendichtemessungen (25,29)
- Die hüftnahen Anteile des Oberschenkelknochens bleiben erhalten, so dass bei einer ggf. notwendigen Wechseloperation optimale Voraussetzungen für alle Arten von Prothesenschäften gegeben sind. Die Ergebnisse (Operationszeit, Blutverlust und Komplikationsrate) entsprechen denen von Erstoperationen mit Standardprothesen (9,22)
- Der Knochenverlust an der Hüftpfanne ist nach Costa (14) nicht größer als bei zementfreien Standardprothesen. Naal et al. (37) geben an, dass der Durchmesser der Pfanne beim Oberflächenersatz etwa 2 mm größer ist.
- Im Gegensatz zu Gleitpaarungen mit Kunststoff (Polyäthylen) kommt es bei der Metall / Metallgleitpaarung zu einer geschmierten Reibung mit extrem wenig Verschleiß.
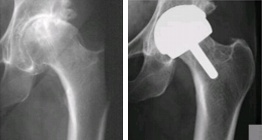
- Abb. 2
Bei einer schlanken, inzwischen 63jährigen Frau, erkennt man 7 Jahre nach Oberflächenersatz die unveränderte Knochendichte und Knochenstruktur am Schenkelhals.
Diese Vorteile machen den Oberflächenersatz (BHR) zu einem geeigneten Verfahren für den jungen, aktiven Patienten. Als Richtlinie gilt ein Alter bis 65 Jahre bei Männern und 60 Jahre bei Frauen.
Nachteile gegenüber Standardprothesen:
- Da der Schenkelhals erhalten bleibt, kann er auch zu einer Schenkelhalsfraktur kommen. Diese seltene Komplikation tritt meistens innerhalb der ersten Monate auf und beruht häufig auf einem Fehler in der Operationstechnik (7,8,10) oder einer zu riskoreichen Indikationsstellung. Bei Nunley (38) findet sich eine Literaturrecherche mit Angaben zu den verschiedenen Kriterien, die die Indikation beeinflussen. Diese Komplikation ist in ihrer Häufigkeit stark abhängig von der Erfahrung des Operateurs. Bei ausreichender Erfahrung liegt die Quote bei 0% bis 2% (43,51).
Im Nationalen Australischen Gelenkersatzregister von 1999 bis 2004 wurden 3497 Oberflächenersatzprothesen (BHR) erfasst, die von 89 Operateuren implantiert wurden. Es wurden 50 Schenkelhalsfrakturen beobachtet. Das entspricht einer Inzidenz von 1,46%, die als gering angesehen werden kann, wenn man berücksichtigt, dass die „Lernkurve“ vieler Chirurgen darin enthalten ist (42). - Lockerung der Femurkomponente auf Grund einer unterbrochenen Durchblutung des Hüftkopfes mit Hüftkopfnekrose. Auch diese Komplikation hängt weitgehend von der Erfahrung des Operateurs ab. Es ist nachgewiesen, dass während der Operation die Durchblutung des Hüftkopfes deutlich vermindert ist. Beim hinteren (dorsalen) Zugang vermindert sich die Durchblutung um 40% (4), die Sauerstoffkonzentration um 60% (44). Doch zeigen Ergebnisse erfahrener Operateure, dass die Hüftkopfnekrose nur sehr selten auftritt, weil sich die Durchblutung offensichtlich ausreichend erholt. McMahon et al. (34) wiesen 26 Monate nach BHR- Oberflächenersatz bei 36 Patienten nach, dass alle Hüftköpfe durchblutet waren.
- Die Beanspruchung der Metall-Metall-Prothesen durch Reibung und die Korrosion im biologischen Milieu führen zu einer Erhöhung der Konzentration von Metallionen und Metallpartikeln. Die Kobalt-Chrom-Molybdän-Legierung führt zu einer Erhöhung der Spiegel von Chrom (Cr³) und Kobalt (Co) im Gewebe. Die Werte für Molybdän (Mo) bleiben fast unverändert. Da diese drei Elemente als Spurenelemente lebenswichtig sind, sind alle drei immer in geringer Konzentration vorhanden. Die chemischen Vorgänge, die der Korrosion zugrunde liegen wurden von Daniel und Kamali (19) beschrieben.
Kobalt ist wesentlicher Bestandteil von Vitamin B12 und von Enzymen, die am Stoffwechsel beteiligt sind.
Chrom ist für den Zuckerstoffwechsel der Zelle erforderlich. Im Gewebe liegt es als 3-wertiges Chrom vor. In dieser Form ist Chrom von der IAEA, der Internationalen Atom-Energie Behörde, als nicht krebserzeugend eingestuft worden. 6-wertiges Chrom stellt ab einer gewissen Konzentration ein potentielles Risiko dar.
Molybdän ist ein wesentlicher Bestandteil vieler Coenzyme. Bei einem Mangel treten Stoffwechselerkrankungen auf.
Die Werte für diese Metalle im Blut und im Urin sind vielfach untersucht worden und sind abhängig von dem Design, der Metallurgie und der Stellung der Implantate. Charakteristisch ist, dass die Werte im Blut und im Urin in den ersten sechs Monaten ansteigen (Einlaufphase) und dann langsam auf einen konstanten Wert abfallen. Die Verläufe der Kurven sind für die Metalle Kobalt und Chrom weitgehend parallel. Nach Daniel und Ziaee (20) steigen die Werte für Chrom bzw. Kobalt von den präoperativen Werten von 0,3 mg/l, bzw. 0,2 mg/l in einem Jahr auf 2,4 mg/l bzw 1,3 mg/l an. Nach sechs Jahren sind sie wieder auf 1,07 mg/l bzw. 1,0 mg/l abgesunken. Je nach Messmethode schwanken diese Werte in anderen Untersuchungen. Die Werte für Molybdän unterscheiden sich kaum von denen bei Menschen ohne Implantate.
Bei Komplikationen oder weniger geeigneten Materialien können diese Werte deutlich erhöht sein.
Kniegelenkendoprothesen mit großen Metalloberflächen erzeugen durch Korrosion ebenso hohe Metallionenspiegel wie die Metall-Metall-Hüftprothesen (32). Diese Tatsache wird von den Kritikern der Metall-Prothesen nicht erwähnt. Während die Metallionenspiegel bei Hüftprothesen regelmäßig im Aufklärungsgespräch erörtert werden, ist dies bei Knieprothesen nur in Ausnahmen der Fall.
Stellen diese erhöhten Werte für Kobalt und Chrom eine Gefahr für die Patienten dar? Folgende Risiken werden genannt:- Nierenerkrankungen: Da die Metallionen durch die Nieren ausgeschieden werden, wird bei Erkrankungen der Niere, die die Ausscheidung der Metallionen einschränken, von Metall-Metall-Prothesen abgeraten.
- Krebs: Seit etwa 50 Jahren werden Metall-Metall-Prothesen implantiert, ohne dass ein erhöhtes Auftreten maligner Erkrankungen beschrieben wurde. Courtland et al. (16) konnten in Tierversuchen nachweisen, dass bei lokaler Applikation von Kobalt, Chrom, Molybdän und Titanlegierungen keine lokalen Tumoren entstanden und andere Tumoren nicht häufiger auftraten als in einer Kontrollgruppe. Visuri et al. (47) veröffentlichten eine statistische Analyse über die Krebshäufigkeit von Patienten mit Metall-Metall-Prothesen nach 15,7 Jahren und Kunststoff-Metall-Prothesen nach 12,5 Jahren sowie einer Kontrollgruppe ohne Prothesen. In einer weiteren Publikation (48) wurden Verläufe von 30 Jahren ausgewertet. Je nach Art des Tumors ist deren Häufigkeit mal etwas größer und mal etwas geringer, ohne statistische Signifikanz. Er kommt zu dem Schluss, dass die geringen Unterschiede in der Häufigkeit von Krebs statistisch nicht signifikant sind und durch andere Faktoren als die Prothesen verursacht werden.
Seit 1990 sind weltweit über 500.000 Metall-Metall-Prothesen implantiert worden, ohne dass es eine wissenschaftliche Publikation erschienen ist, die eine bösartige Erkrankung in Zusammenhang mit einer Metall-Metall-Prothese bringt. - Allergien: Allergische Reaktionen der Haut auf Metalle, besonders auf Nickel und Chrom sind sehr häufig. Die Hautärzte geben die Häufigkeit mit 10% bis 20% an. Im Körper sind allergische Reaktionen dagegen sehr selten. Allerdings sind positive Allergietests bei Trägern von Metall-Metall-Prothesen häufiger, besonders in Fällen von Implantatversagen. Da alle Metalle im Körper der Korrosion ausgesetzt sind, werden Metallionen freigesetzt, die sich mit Eiweiß verbinden und dann das Immunsystem aktivieren können. Die klinische Bedeutung dieser Vorgänge ist nicht ausreichend geklärt. Shimmin und Back (43) fanden unter 3.497 Patienten nur einen Fall, bei dem eine Revision bei dem Verdacht auf eine allergische Reaktion vorgenommen wurde. Daniel und Ziaee (20) berichten, dass von über 3.500 Patienten bei einer Frau wegen eines Ekzems der Verdacht auf eine Allergie bestand. Die erfolgreiche Therapie mit Medikamenten und das jährlich auftretende Rezidiv sowie der weitere Verlauf sprechen eher dafür, dass es sich um kein allergisches Geschehen handelte.
Auffällig ist, dass bei Knieprothesen allergische Reaktionen kaum eine Bedeutung zu haben scheinen.
Willert et al. (50) beschreiben feingewebliche Befunde von periartikulärem Gewebe von Revisionen bei Metall-Metall-Prothesen. Die Revisionen erfolgten wegen Schmerzen und Gelenkergüssen und bei den meisten wegen Lockerung einer oder beider Komponenten. Die Anreicherung und Verteilung bestimmter Zellen, wie sie auch von Davies (21) beschrieben werden, werden mit dem Akronym „ALVAL“ (Aseptic Lymphocytic Vasculitis and Associated Lesions) zusammengefasst. Es wird festgestellt, dass diese Veränderungen für Partikel dieser Metalle charakteristisch sind. Untersucht wurden aber Gewebeproben aus der Umgebung von Prothesen, die versagt und vermehrt Partikel freigesetzt hatten.
Über Pseudotumoren in 1,8% ihrer 1.419 Fälle berichten Glyn-Jones et al. (24). Die Häufigkeit hängt vom Alter, Geschlecht, von der Diagnose und Größe der Prothese ab. Frauen, die kleinere Prothesen benötigen, Patientinnen unter 40 Jahren und Patienten mit Arthrosen bei Dysplasien haben nach diesen Untersuchungen ein höheres Risiko, dass eine Prothese gewechselt werden muss. Die Autoren halten eine allergische Ursache für möglich.
Andere Autoren fanden keine größere Zahl derartiger Komplikationen.
Eine wissenschaftlich eindeutige Erklärung gibt es zurzeit nicht. Die Ursache für die unterschiedliche Häufigkeit wird weiter untersucht.
Forscher aus dem „Dorr Arthritis Institute“ (31,41) kommen nach Untersuchungen an nicht gelockerten Prothesen zu der Ansicht, dass es sich eher um eine toxische Reaktion handelt, wenn das Gewebe durch vermehrten Abrieb mit Metall überladen wird. Sie führen an, dass es in der Literatur nicht einen Fall gibt, bei dem speziell wegen der nachgewiesenen Diagnose einer Allergie ein Prothesenwechsel durchgeführt wurde. Im Australischen Prothesenregister werden Allergien als Revisionsgrund erwähnt. Wie diese allergischen Reaktionen nachgewiesen wurden, wird nicht beschrieben. - Schwangerschaft und Metallprothesen. Als Argument gegen die Anwendung der Metall-Metall-Prothesen bei Frauen mit Kinderwunsch wird angeführt, dass die erhöhten Metallspiegel der Mutter dem Kind schaden könnten. Untersuchungen an Schwangeren mit und ohne Metall-Metall-Prothesen zeigten, dass im Blut der Nabelschnur die Spiegel für Kobalt- und Chromionen für beide Gruppen gleich sind. Da beide Elemente als Spurenelemente für die Entwicklung des Kindes unentbehrlich sind lässt die Plazenta als eine Barriere nur die Menge an Metallionen durch, die das Kind benötigt (52). Es gibt also keinen Anhalt dafür, dass das Kind durch die Metall-Metall-Prothese der Mutter geschädigt wird. Da in den ersten sechs bis zwölf Monaten die Metallspiegel erhöht sind, sollte eine Schwangerschaft erst nach Ablauf dieser Frist eintreten. Die Metallionenspiegel in der Muttermilch sind nicht bekannt. Es ist zu erwarten, dass sie den Blutwerten entsprechen. Da nur ca. 0,4% parenteral resorbiert werden, erscheint eine Schädigung kaum möglich (Ziaee, mündl. Mitt.).
- Vernünftig ist es sicher, bei Kinderwunsch mit dem Gelenkersatz bis nach der Schwangerschaft zu warten. Tritt eine Schwangerschaft bei bestehendem Oberflächenersatz ein, soll der Metallionenspiegel kontrolliert und die Untersuchungen in der Schwangerschaft sorgfältig durchgeführt werden.
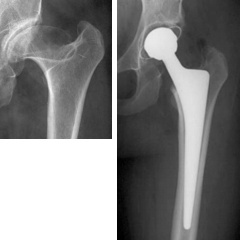
Beispiele für die Anwendung des Oberflächenersatzes (BHR):
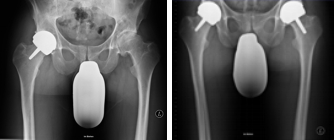
- Abb. 1
Die Primäre Coxarthrose bei Männern bietet die besten Voraussetzungen für den BHR Oberflächenersatz.
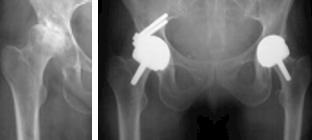
- Abb. 2 / Abb. 3
Rechte Hüfte: Verlagerung des Hüftkopfes nach oben mit Beinverkürzung. Wiederherstellung der Hüftpfanne und der Beinlänge durch die verschraubte Dysplasiepfanne und Defektauffüllung mit Knochen.
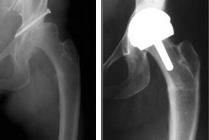
- Abb. 4
Nach Korrekturoperationen am Becken und am Oberschenkel ist eine Deformation entstanden, die die Anwendung einer Standardprothese ohne erneute Durchtrennung (Osteotomie) des Oberschenkels unmöglich macht.
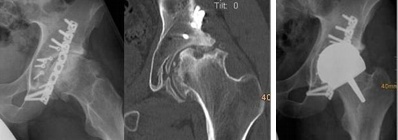
- Abb. 5
Bruch der Hüftpfanne bei einem 22 jährigen Mann. Im weiteren Verlauf nach Operation Zerstörung des Gelenkes und Knochenverluste am Hüftkopf. Bei dem jungen Mann wurde der gesunde Rest des Hüftkopfes durch den Oberflächenersatz erhalten.
2. Standardprothesen mit Metall / Metall, Keramik / Keramik oder Kunststoffpfannen mit Metall- oder Keramikköpfen

- Abb. 11: Die Hart-Hart-Gleitpaarungen aus Metall oder Keramik oder Kombinationen mit Kunststoff (Polyäthylen), der auch mit Zirkoniumoxid (Oxinium) kombiniert werden kann, erlauben eine Anpassung an die Bedürfnisse des Patienten.
Ist bei ausgedehnten Zerstörungen des Kopf-Halssegmentes oder Osteoporose oder auf Grund des Allgemeinzustandes des Patienten und seines Aktivitätsniveaus der Oberflächenersatz nicht indiziert, so stellen Standardprothesen mit verschiedenen Gleitpaarungen und Schaftformen gute Alternativen dar, denn seit der Einführung des Oberflächenersatzes BHR 1996 sind auch bei den Schaftprothesen bedeutende Fortschritte erzielt worden.
Die jetzt zur Verfügung stehenden Keramiken haben eine sehr hohe Bruchfestigkeit, so dass ein Bruch extrem unwahrscheinlich ist. Diese Bruchfestigkeit ermöglichte eine größere Dimensionierung der Komponenten, so dass die Luxationsgefahr auch bei diesen Prothesen deutlich geringer geworden ist. Die Abriebfestigkeit der Keramik lässt eine sehr hohe Lebensdauer erwarten.
Durch die deutliche Verbesserung der Abriebfestigkeit des Kunststoffes Polyethylen (Hochvernetzte PE, Imprägnierung mit Vitamin E), stellen Pfannen mit diesem Gleitpartner ebenfalls eine langlebige Alternative dar.
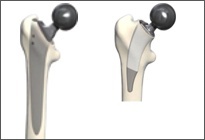
- Abb. 12a und 12b
Abb. 12a:
Standardschäfte, zementiert oder zementfrei, führen zu einer Umleitung des Kraftflusses vom Becken auf den Oberschenkel. Abhängig vom Design ist der Um- und Abbau des Knochens (stress shielding) unterschiedlich ausgeprägt.
Abb. 12b:
Kurzschaftprothesen sollen den Kraftfluss weniger beeinflussen.
- Abb. 15
Zementfreier Schaft mit einer modernen Keramik-Keramik-Gleitpaarung, die auch größere Komponenten mit hoher Luxationssicherheit erlaubt. Die hohe Bruchfestigkeit der Mischkeramik bietet auch bei großen Belastungen Sicherheit.
- Abb. 16
Bei einer Beinverkürzung durch angeborene oder erworbene Deformitäten von 3 bis 4 cm kann eine Korrektur nur mit einem Standardschaft erfolgen. In diesem Fall eine Metall-Metall-Gleitpaarung mit kleinem Kopf.
Warum werden heute Metall-Metall-Gleitpaarungen für den Oberflächenersatz angewendet?
1) Die Geschichte der Metall-Metall-Gleitpaarung
Schon 1938 wurde die Kobalt-Chrom-Molybdän-Legierung als Implantatwerkstoff eingeführt. Die ersten Hüftgelenksendoprothesen hatten diese Gleitpaarung, so dass es sehr lange Erfahrungen gibt. Schon in den 50ger Jahren wurden Metall-Metall-Prothesen implantiert. Sie bestanden aus derselben Kobalt-Chrom-Molybdän-Legierung, die auch heute wegen ihrer guten tribologischen Eigenschaften (geringe Reibung, geringer Abrieb) benutzt wird. Die bekanntesten Prothesen waren die von Peter Ring und die von McKee-Farrar. Letztere wurde auch in großer Zahl in Deutschland verwendet. Die ungünstigere Form des Prothesenstiels, die unzureichende Operationstechnik, die Schwierigkeiten bei der Verarbeitung des sehr harten Materials und die fehlende Präzision in der Fertigung führten zu vielen Komplikationen, so dass die Anwendung zu Gunsten der Kunststoff-Metall-Gleitpaarung von Charnley (low friction) aufgegeben wurde. Ein besseres Design des Prothesenstiels, die standardisierte Operationstechnik und die mittelfristig weniger komplikationsträchtige Gleitpaarung waren die Gründe für diesen Wechsel (5,6).
Im Laufe der Zeit stellte sich aber heraus, dass ein Teil der Patienten mit den McKee-Farrar-Prothesen und einzelne mit den Ring-Prothesen auch nach über 30 Jahren keine Lockerungen der Prothese und keinen erkennbaren Abrieb mit Zerstörung des knöchernen Lagers zeigten (27,39).
Prothesen, die nach dem Tod von Patienten untersucht wurden, zeigten einen extrem geringen Verschleiß von etwa 0,5 bis 1,0 µm pro Jahr und Komponente. Das Abriebvolumen war also um den Faktor 100 geringer als bei dem Kunststoff Polyäthylen, der heute noch, allerdings mit verbesserter Abriebfestigkeit, verwendet wird.
2) Die heutigen Metall-Metall-Gleitpaarungen
Ende der 80er Jahre führten diese Ergebnisse der Metall-Metall-Prothesen zu der Erkenntnis, dass diese Gleitpaarung der Gleitpaarung mit Polyäthylen grundsätzlich überlegen ist, wenn die Prothesen bestimmten Standards in der Herstellung entsprechen (40) und die Implantation mit der korrekten Positionierung der Komponenten erfolgt.
Für Standardprothesen wurde deshalb die Metall-Metall-Gleitpaarung 1989 wieder eingeführt (49).
Das bestechende Konzept des Oberflächenersatzes ist nicht neu. Nach den Misserfolgen von Charnley mit Pfannen aus Teflon wurde die Idee des Oberflächenersatzes in Deutschland zuerst von Wagner mit Pfannen aus Polyäthylen wieder aufgegriffen. Auch in anderen Ländern wurden ähnliche Prothesen verwendet (15).
Die enttäuschenden, nicht akzeptablen Ergebnisse des Oberflächenersatzes mit Polyäthylenpfannen mit etwa 50% Lockerungen nach 5-6 Jahren beruhten auf dem ungeeigneten Material der Pfanne, durch das sehr hoher Abrieb entstand, der wiederum zur Zerstörung des Knochens (Osteolysen) führte (26).
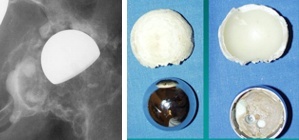
- Abb. 17a und 17b
Abb. 17a: Das Röntgenbild zeigt die Reste von Knochenzement, die zerriebene Pfanne und die ausgedehnte Zerstörung des Knochens am Oberschenkel und am Becken durch Kunsstoffpartikel (Osteolysen).
Abb. 17b: Die durch Abrieb zerstörte Kunststoffpfanne und die beschädigte Oberfläche des Metallkopfes.
Anfangs glaubte man, dass die Misserfolge auf die unterbrochene Durchblutung des Hüftkopfes mit anschließendem Absterben des Knochens zurückzuführen seien.
Untersuchungen von Hüftköpfen nach Oberflächenersatz zeigten jedoch, dass der Knochen unter einer zementierten Kappe nur sehr selten abstirbt (11). Campbell et al. (12) fanden unter 25 Hüftköpfen, die 12 Jahre nach Oberflächenersatz untersucht wurden, keine, die abgestorbenen waren. Das Versagen des Oberflächenersatzes der 70er Jahre beruhte also nicht auf einer Durchblutungsstörung des Hüftkopfes, sondern auf dem ungeeigneten Material. Die raue Oberfläche des Kunststoffes erlaubt keine „geschmierte Reibung“, so dass bei großen Hüftköpfen die große Oberfläche und die große Geschwindigkeit der Gleitpartner den Abrieb stark vermehrten, wodurch die Lockerung der Prothese mit Zerstörung des knöchernen Lagers beschleunigt wurde. Diese Nachteile sind die Ursache dafür, dass bei Kunststoff möglichst kleine Prothesenköpfe verwendet werden, um den Abrieb zu vermindern. Der Nachteil der kleinen Hüftköpfe ist das erhöhte Luxationsrisiko.
Anerkannt ist, dass die folgenden Kriterien für den Erfolg der Metall-Metall-Gleitpaarung entscheidend sind:
- Der Spalt zwischen dem Hüftkopf und dem Inneren der Pfanne (Clearence) darf nicht zu klein sein, weil es sonst zu einem Kontakt am Pfannenrand mit erhöhtem Abrieb und zu einem Drehmoment auf die Pfanne kommt, das zur Lockerung führen kann (49). Die Legierung soll einen hohen Kohlenstoffanteil aufweisen, weil die dadurch entstehenden Karbide in der Oberfläche deren Härte und damit die Abriebfestigkeit erhöhen (13).
- Die meistens verwendeten Gusslegierungen sollen nach dem Aushärten zur weiteren Bearbeitung nicht wieder erhitzt werden, weil dadurch die Metall-Kohlenstoff-Verbindungen (Karbide) an der Oberfläche zerstört werden (13).
- Die Komponenten müssen absolut rund sein; Die Rauigkeit der Oberfläche muss nach der Einlaufphase so gering sein, dass ein Schmierfilm zwischen Kopf und Pfanne entsteht, der den Verschleiß vermindert.
Die Erkenntnis, dass mit einer Metall-Metall-Gleitpaarung grundsätzlich gute Ergebnisse zu erzielen waren, führte dazu, dass McMinn auch die bestechende Idee des Oberflächenersatzes 1989 wieder aufnahm und nach einer Entwicklungsphase 1996 die Erfahrung mit 235 Implantationen vorstellte. Es kam zu keiner Schenkelhalsfraktur oder Hüftkopfnekrose. Bei den 116 Prothesen, die nach der heutigen Technik operiert wurden, mit einer zementfreien Pfanne und einer zementierten Femurkomponente, musste bei einer Beobachtungszeit von durchschnittlich 8,3 Monaten keine Prothese gewechselt werden (35).
In den folgenden Jahren wurden von der Arbeitsgruppe um McMinn, aber auch von anderen Anwendern des „Birmingham Hip Resurfacing“ überzeugende Ergebnisse veröffentlicht. Daniel et al. (17) aus dem McMinn Centre, berichteten über 384 Patienten, Durchschnittsalter 48,3 Jahre, mit 446 Prothesen (BHR), die nach 1,1 bis 8,2 Jahren untersucht wurden. Sechs Patienten waren unabhängig von der Hüftoperation verstorben. Von den 440 Prothesen musste eine wegen einer Hüftkopfnekrose gewechselt werden. Treacy et al. (46) berichteten über die Ergebnisse von 130 Patienten, Durchschnittsalter 52,1 Jahr, mit 144 Oberflächenersatzprothesen (BHR) nach 5 Jahren. Drei Prothesen wurden gewechselt, zwei wegen eines Infektes und eine wegen einer Hüftkopfnekrose.
Steffen et al. (45) stellte die Ergebnisse von 532 Patienten, Durchschnittsalter 51,8 Jahre mit 610 Prothesen (BHR) vor. Die sieben Fachärzte und 30 Ärzte in der Ausbildung gehörten nicht zu den Entwicklern der Prothese, waren also unabhängig. Da außer der primären Coxarthrose auch Coxarthrosen bei Dysplasie und Hüftkopfnekrosen, mit einem höheren Risiko, operiert wurden, ist die Erfolgsrate von 95% nach sieben Jahren sehr zufriedenstellend.
Eine prospektive Multicenter Studie mit 679 Operationen, durchgeführt von 60 Chirurgen in mehreren Kliniken zeigt nach fünf bis acht Jahren eine Überlebensrate der Prothesen von 95,7%. Die Studie begann 1997, als nur spärliche Erfahrungen mit der Operationstechnik vorlagen. Unter Berücksichtigung der Zahl der Operateure und der „Lernkurve“ für dieses Verfahren, ist das Ergebnis durchaus als gut zu bezeichnen (28).
Verglichen mit Standardprothesen geben die meisten Autoren an, dass das Aktivitätsniveau der Patienten nach Oberflächenersatz höher ist und viele Patienten sehr belastende Berufe und Sportarten ausüben (17,30,46). Andere Autoren fanden keine wesentlichen Unterschiede zu Standardprothesen mit großen Prothesenköpfen.
Mont et al. (36) wiesen nach, dass die Komplikationsrate nach über drei Jahren nicht höher ist als bei Standardprothesen.
Aus den Nationalen Prothesenregistern Schwedens (2) und Australiens (1) lässt sich ablesen, dass die Komplikationsrate nach dem BHR-Oberflächenersatz höher ist, wenn alle Altersgruppen eingeschlossen werden. Betrachtet man aber die Zielgruppe der unter 50jährigen, dann sind die Ergebnisse der BHR deutlich besser, die Haltbarkeit nach 16 Jahren bei Standardprothesen betrug bei über 75jährigen 95%, bei unter 50jährigen aber nur 70%. Die geringere Zahl von Infektionen und Luxationen beim Oberflächenersatz ist in diesen Zahlen noch nicht berücksichtigt.
Seit 1996 sind über 160.000 Original - Oberflächenersatzprothesen (BHR) mit sehr guten Ergebnissen implantiert worden, ohne dass Änderungen an dem Implantat vorgenommen werden mussten. Dem entsprechen auch unsere eigenen Erfahrungen mit fast 2.500 Anwendungen bis 2009.
Auf Grund dieser Ergebnisse wurde das Verfahren von den meisten Herstellern von Endoprothesen, mehr oder weniger modifiziert, kopiert. Diese Änderungen des Designs und der Metallurgie führten aber zu schlechteren Ergebnissen, wie im Australischen Nationalen Register festgestellt wurde (1).
Das Gebiet der Endoprothetik mit seinen vielen Modellen und Biomaterialien kann mit diesen Ausführungen nicht umfassend dargestellt werden. Es sollten Ihnen jedoch einige Informationen mit dem Schwerpunkt „knochensparende Prothesen“ und „Metall-Metall-Gleitpaarungen“ vermittelt werden. Die Literaturangaben sind nur ein kleiner Teil der inzwischen vorliegenden Veröffentlichungen. Sie sollen Ihnen zeigen, dass diese Informationen auf wissenschaftlichen Veröffentlichungen beruhen und nicht eine subjektive Meinung darstellen.
Leider werden in den Medien häufig sehr einseitige, irreführende und oberflächliche Darrstellungen, die einer Werbung sehr ähnlich sind, angeboten. Werbeähnlichen Charakter hatten besonders zwei Sendungen des Gesunheitsmagazins „Visite“ am 16.09.2008 und am 03.11.2009.
In der ersten wurde eine angebliche „Weiterentwicklung“ des Originalimplantates von McMinn von Prof. Dr. Scholz, Berlin und PD Dr. Gerdesmeyer, Kiel, angepriesen, ohne dass relevante Ergebnisse vorgestellt wurden. Zu demselben Thema, mit gleicher Aussage, wurde auch die Sendung „Quivive“ im RBB am 20.05.2009 ausgestrahlt. Kritische Fragen wurden von den Moderatorinnen nicht gestellt. Diese „Weiterentwicklungen“ sind inzwischen nicht mehr erhältlich.
In der Sendung „Visite“ des NDR am 03.11.2009 wurde von Herrn Dr. S. Oehme, Chefarzt Orthopädie, Ostseebad Damp, die Behauptung aufgestellt, dass der Oberflächenersatz eine Komplikationsrate von über 15% aufweise. Eine Quelle für diese Behauptung wurde nicht angegeben. Gleichzeitig wurde angedeutet, dass deshalb der Oberflächenersatz in den USA vom Markt genommen werden solle. Auch diese Behauptung ist falsch.
Aus demselben Klinikkonzern (Damp-Holding, Hamburg, jetzt Helios-Klinikum) werden in der Presse Anzeigen aufgegeben, die ebenfalls 15% Komplikationen angeben. Quellen werden nicht genannt. Angaben darüber, um welchen Oberflächenersatz es sich handelt, werden nicht gemacht. Es werden mindestens 15 verschiedene Modelle angeboten.
Im Spiegel 45/2009 wird von der Autorin Fr. Dr. V. Hackenbroch festgestellt: „ mit dem derzeitigen McMinn Modell aber gibt es bislang nicht mehr als sieben Jahre Erfahrung“. Welches ist das „derzeitige McMinn Modell“? Es sind mindestens 15, sehr unterschiedliche Modelle verfügbar! 1996 wurden die ersten Fälle veröffentlicht. Auf dem Europäischen Orthopädenkongress 2009 in Wien wurden 11-Jahresergebnisse aus Birmingham vorgestellt. Von 403 Patienten mussten zwei Prothesen wegen Komplikationen gewechselt werden. Die Überlebensrate beträgt 99,7%. Derartige Ergebnisse kann nicht jeder Operateur erzielen, sie sind aber grundsätzlich möglich. Weitere Studien sind jedem Interessenten zugänglich.
Der Leser oder Zuschauer, muss sich darüber im Klaren sein, dass die Recherchen in den Medien sehr oberflächlich und die vertretenen Meinungen deutlich tendenziös sind.
Literatur:
- Australian Orthopaedic Association National Joint Replacement Registry Annual Report. Adelaide:AOA; 2009
- Swedish Hip Arthroplasty Register Annual Report 2006
- National Joint Registry for England and Wales. 4th Annual Report 2007
- Amarasekara HW, Costa ML, Foguet P, Krikler SJ, Prakash U, Griffin DR: The Blood Flow to the Femoral Head/Neck Junction During Resurfacing Arthroplasty. J Bone Joint Surg 2008; 90-B: 442
- Amstutz HC: History of Metal-on-Metal Articulations including Surface Arthroplasty of the Hip. In: Rieker C, Oberholzer S, Wyss U (ed): World Tribology Forum in Arthroplasty. Huber 2001
- Amstutz HC, Grigoris P: Metal-on-Metal Bearings in Hip Arthroplasty. Clin Orthop 1996; 329 S: 11
- Amstutz HC, Campbell PA, Le Duff M: Fracture of the Neck of the Femur After Surface Arthroplasty of the Hip. J Bone Joint Surg 2004; 86-A: 1874
- Anglin C, Engh P, Masri BA, Tonetti J, Hodgson AJ,Eng P, Greidanus NV: Hip Resurfacing Femoral Neck Fracture Influenced by Valgus Placement. Clin Orthop 2007; 465: 71
- Ball ST, Le Duff M, Amstutz HC: Early Results of Conversion of a Failed Femoral Component in Hip Resurfacing Arthroplasty. J Bone Joint Surg 2007; 89-A: 735
- Beaulé PE, Campbell PA, Hoke R, Dorey F: Notching of the Femoral NeckDuring Resurfacing Arthroplasty of the Hip. A Vascular Study. J Bone Joint Surg 2006; 88-B:35
- Bradley GW, Freeman MAR, Revell PA, Path MRC: Resurfacing Arthroplasty, Femoral Head Viability. Clin Orthop 1987; 220: 137
- Cambpell P, Mirra J, Amstutz HC: Viability of Femoral Heads Treated with Resurfacing Arthroplasty. J Arthroplasty 200; 15: 120
- Cawley J, Metcalf JEP, Jones AH, Band TJ, Skupien DS: A Tribological Study of Cobalt Chromium Molybdenum Alloys Used in Metal-on-Metal resurfacing Hip Arthroplasty. Wear 2003; 255:999
- Costa M, Prakash U, Forguet P: Comparison of Cup Sizes in Uncemented and Resurfacing Arthroplasty. J Bone Joint Surg 2009; 91-B Suppl I: 15
- Cotella L, Railton GT, Nunn D, Freeman MAR, Revell PA: ICLH Double-cup Arthroplasty, 1980-1987. J Arthroplasty 1990; 5: 349
- Courtland GL, Sundermann W: Metal Carcinogenesis in Total Joint Arthroplasty. Animal Models. Clin Orthop 1996; 329 S: 264
- Daniel J, Pynsent PB, McMinn DJ: Metal-on-Metal Resurfacing of the Hip in Patients under the Age of 55 Years with Osteoarthritis. J Bone Joit Surg 2004; 86-B: 177
- Daniel J, Pradhan C, Ziaee H, McMinn DJW: A Clinicoradiologic Study of the Birmingham Mid-Head Resection Device. Orthopedics 2008; 31:124
- Daniel J, Kamali A: Corrosion and Its Contribution to Metal Release. In: D.McMinn (ed.) Modern Hip Resurfacing. Springer-Verlag London 2009
- Daniel J, Ziaee H: Metal Ions. In: D.McMinn (ed.) Modern Hip Resurfacing. Springer-Verlag London 2009
- Davies AP, Willert H-G, Campbell PA, Learmonth ID, Case CP: An Unusual Lymphocytic Perivascular Infiltration in Tissues Around Contemporary Metal-on-Metal Joint Replacements. J Bone Joint Surg 2005; 87-A: 18
- Garrett SJW, Bolland BJ, Yates PJ, Latham JM: Revision of the failed femoral Resurfacing Component: Is it Successful? J Bone Joint Surg2008; 90-B Suppl III: 544
- Glyn-Jones, Gill HS, McLardy-Smith, Murray DW: Roentgen Stereophotogrammetric analysis of the Birmingham Hip Resurfacing Arthroplasty. A Two Year Study. J Bone Joint Surg 2004; 86-B:172
- Glyn-Jones S, Pandit H, Kwon Y-M ,Doll H, Gill HS, Murray DW: Risk Factors for Inflammatory Pseudotumor Formation Following Hip Resurfacing. J Bone Joint Surg 2009; 91-B: 1566
- Hayaishi Y, Miki M, Nishii T, Hananouchi T, Yoshikawa H, Sugano N: Proximal Femoral Bone Density After Resurfacing Arthroplasty and After Standard Stem-Type Cementless Total Hip Arthroplasty, Both Having Similar Neck Preservation and the same Articulation Type. J Arthroplasty 2007; 22: 1208
- Howie DW, Cambell D, McGee M, Cornish BL: Wagner Resurfacing Hip Arthroplasty. The Results of One Hundred Consecutive Arthroplasties After Eight to Ten Years. J Bone and Joint Surg 1990; 72-A: 708
- Jacobsson SA, Djerf K, Wahlström O: 20-Year Results of McKee-Farrar Versus Charnley Prosthesis. Clin. Orthop 1996; 329 S: 60
- Khan M, Kuiper J-H, Edwards D, Robinson E, Richardson JB: Birmingham Hip Arthroplasty. Five to Eight Years of Prospective Multicenter Results. J Arthroplasty 2009; 24: 1044
- Kishida Y, Sugano N, Nishii T, Miki H, Yamaguchi K, Yoshikawa H: Preservation of Bone Mineral Density of the Femur After Surface Replacement of the Hip. J Bone Joint Surg 2004; 86-B: 185
- Lingard EA, Muthumayandi K, Holland JP: Comparison of Patient-Reported Outcomes between Hip Resurfacing and Total Hip Replacement. J Bone Joint Surg 2009; 91-B: 1550
- Long WT, Dorr LD, Gendelman V: An American Experience with Metal-on-Metal Total Hip Arthroplasty. J Arthroplasty 2004: 19 Suppl 3: 29
- Luetzner J, Krummenauer F, Lengel AM, Ziegler J, Witzleb WC: Serum Metal Ion Exposure after Total Knee Arthroplasty. Clin. Orthop 2007; 461: 136
- Lundberg A, Itayem R: Migration Studies. In: D.McMinn (ed.) Modern Hip Resurfacing. Springer-Verlag London 2009
- McMahon SJ, Young D, Ballok Z, Badaruddin BS, Larbpaiboonpong V, Hawdon G: Vascularity of the Femoral Head After Birmingham Hip Resurfacing. A Technetium Tc 99m Bone Scan/Single Photon Emission Computed Tomography Study. J Arthroplasty 2006; 21: 514
- McMinn D, Treacy R, Lin K, Pynsent P: Metal on Metal Surface Replacement of the Hip, Experience of the McMinn Prosthesis. Clin Orthop 1996; 329 S: 89
- Mont MA, Marker DR, Smith JM, Ulrich SD, McGrath MS: Resurfacing is comparable to Total Hip Arthroplasty at Short-term Followup. Clin Orthop 2009; 467: 66
- Naal FD, Kain MSH, Hersche O, Munzinger U, Leunig M: Does Hip Resurfacing Require Larger Acetabular Cups Than Conventional THA? Clin Orthop 2009; 467: 923
- Nunley RM, Della Valle CJ, Barrack RL: Is Patient Selection Important for Hip Resurfacing? Clin Orthop 2009; 467: 56
- Schmalzried TP, Szuszczewicz E S, Akizuki K H, Petersen T D, Amstutz HC: Factors Correlating With Long Term Survival of McKee-Farrar Total Hip Prostheses. Clin Orthop 1996; 329 S: 48
- Schmidt M, Weber H, Schön R: Cobalt Chromium Molybdenum Metal Combination for Modular Hip Prostheses. Clin Orthop 1996; 329 S. 35
- Shahrdar C, Campbell P, Mirra J, Dorr LD: Painful Metal-on-Metal Total Hip Arthroplasty. J Arthroplasty 2006; 21: 289
- Shimmin A, Back DL, Young D: Evaluation of the Learning Curve Associated with Hip Resurfacing: A National Review of 50 Cases. J Bone Joint Surg 2005; 87-B, Supp I: 45
- Shimmin AJ, Back D: Femoral Neck Fractures Following Birmingham Hip Resurfacing. J Bone Joint Surg 2005; 87-B: 463
- Steffen RT, Smith SR, Urban JPG, McLardy-Smith P, Beard DJ, Gill HS, Murray DW: The Effect of Hip Resurfacing on Oxygen Concentration in the Femoral Head. J Bone Joint Surg 2005; 87-B: 1468
- Steffen RT, Pandit HP, Palan J, Beard DJ, Gunle R, McLardy-Smith P, Murray DW, Gill HS: The Five-Year Results of the Birmingham Hip Resurfacing Arthroplasty: An Independent Series: J Bone and Joint Surg 2008; 90-B: 436
- Treacy RBC, McBryde CW, Pynsent PB: Birmingham Hip Resurfacing Arthroplasty. A Minimum Follow-Up of Five Years. J Bone and Joint Surg 2005; 87-B: 167
- Visuri T, Pukkala E, Paavolainen P, Pulkkinen P, Riska EB: Cancer Risk After Metal on Metal and Polyethylene on Metal Total Hip Arthroplasty. Clin Orthop 1996; 329 S: 280
- Visuri T, Pukkala E: Does Metal-on-Metal Total Hip Prosthesis Have Influence on Cancer? A Long-Term Follow-up Studie. In: Rieker C, Oberholzer S, Wyss U (ed): World Tribology Forum in Arthroplasty. Huber 2001
- Weber B G: Experience with the Metasul Total Hip Bearing System. Clin Orthop. 1996; 329 S: 69
- Willert H-G, Buchhorn GH, Fayyazi A, Flury R, Windler M, Köster G, Lohmann CH: Metal-on-Metal Bearings and Hypersensitivity in Patients with Artificial Hip Joints. A Clinical and Histomorphological Study. J Bone Joint Surg 2005; 87-A: 28
- Witjes S, Smolders MH, Beaulé PE, Pasker P, Van Susante LC: Learning from the Learning Curve in Total Hip Resurfacing: A Radiographic Analysis. Arch Orthop Trauma Surg 2009
- Ziaee H, Daniel J, Datta AK, Blunt S, McMinn DJ: Transplacental Transfer of Cobalt and Chromium in Patients with Metal-on-Metal Hip Arthroplasty: A Controlled Study. J Bone Joint Surg 2007; 89-B: 301